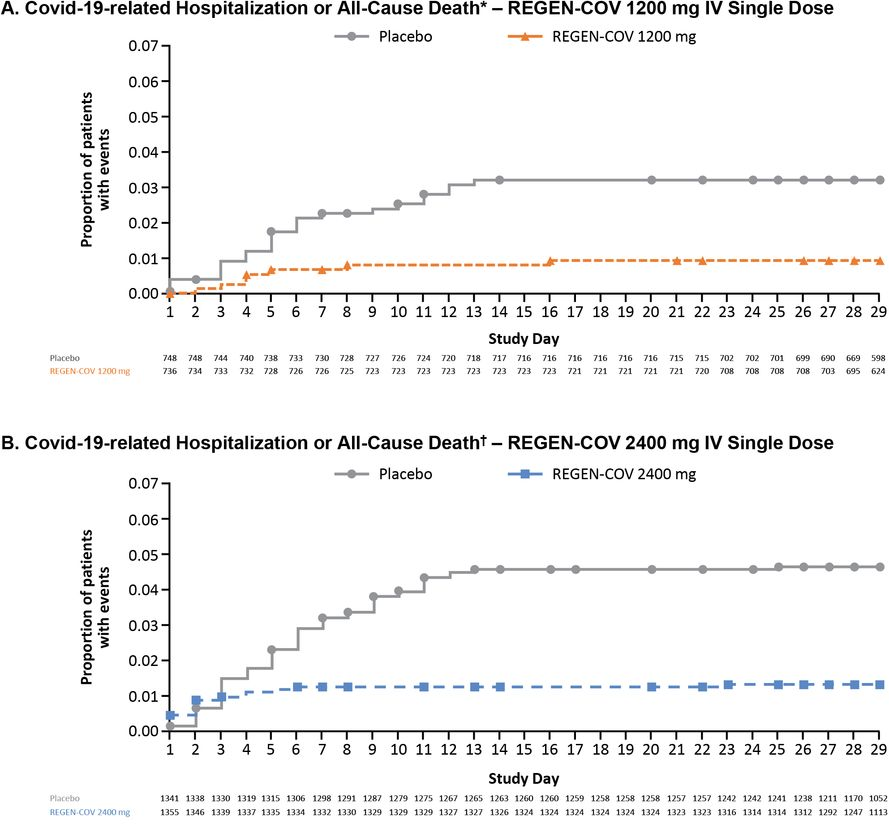
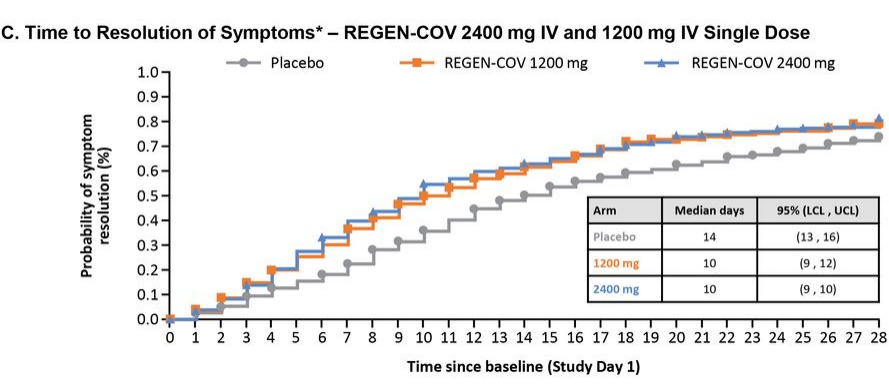
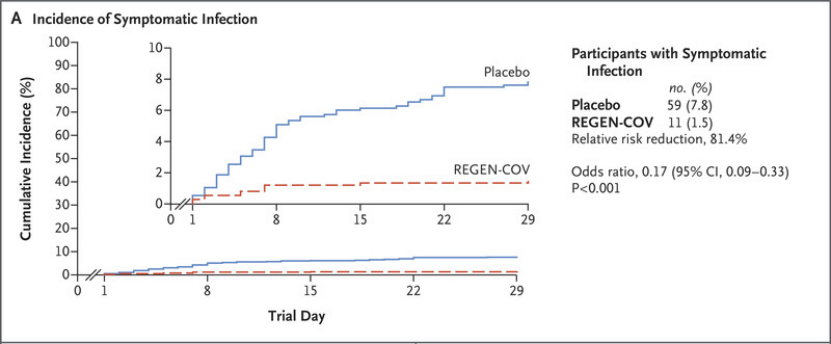
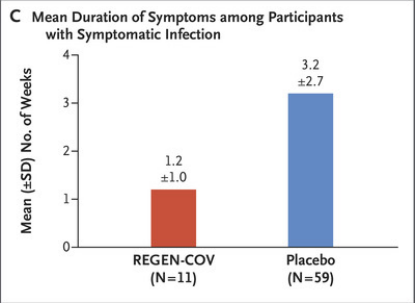
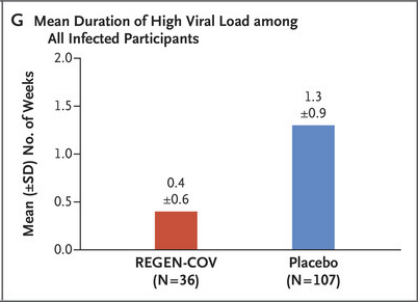
近日,FDA扩大了对REGEN-COV的紧急授权范围,允许REGEN-COV用于有高风险发展为严重COVID-19的人群进行暴露后预防性治疗[1]。相关研究也被发表在NEJM进行报道。也就是说,REGEN-COV是美国目前唯一可同时用于COVID-19治疗与预防的抗体疗法。REGEN-COV(以前称为REGN-COV2),是由casirivimab和imdevimab两种中和抗体组成的双抗体疗法。值得一提的是,REGEN-COV也是第一个获得FDA紧急使用授权的联合疗法。另一获紧急授权的中和抗体组合疗法的是我国君实生物和礼来联手开发的etesevimab和bamlanivimab组合。再生元制药公司在2021年美国胸科学会国际会议(ATS 2021)中表示,REGEN-COV能显著降低COVID-19门诊患者的住院或全因死亡的风险,迅速缓解感染症状,并降低病毒载量。该研究[2]发表在medRxiv杂志:研究人员将4057名受试者分为三组,随机分配接受安慰剂、REGEN-COV 1200mg或REGEN-COV 2400mg,受试患者均具有≥1个严重COVID-19危险因素,核酸检测为阳性。结果表明,REGEN-COV显著降低了COVID-19相关的住院或全因死亡率,2400mg剂量组降低了71.3%,p<0.0001;1200mg剂量组降低了70.4%,p=0.0024。图示COVID-19相关住院或全因死亡情况,可以看到REGEN-COV组曲线(A黄色,B蓝色)明显低于安慰剂组。REGEN-COV组症状消退的中位时间较安慰剂组缩短了4天,2400mg和1200mg两个剂量的症状消退中位时间为10天,安慰剂组为14天,p<0.0001。图示症状消退人数的时间变化曲线,可以看出REGEN-COV两剂量组(1200mg黄色,2400mg蓝色)症状消退人数比例均较安慰剂组(灰色)高。同时,与安慰剂组相比,REGEN-COV两剂量组都能更快地降低病毒载量;引发的不良反应事件发生率更低,1200mg为1.1%,2400mg为1.3%,安慰剂组为4.0%。总的来说,这项研究证明了静脉注射REGEN-COV对COVID-19门诊患者有一定的治疗作用,同时其安全性也得到了保证。在确定了REGEN-COV的治疗作用后,再生元对REGEN-COV的预防保护作用及其他给药方式进行了进一步的研究,皮下注射REGEN-COV预防新冠病毒感染的试验结果于8月4日发表在NEJM[3]:研究表示,REGEN-COV能降低暴露于病毒后未感染者的感染风险,也再次证明了REGEN-COV能减少症状持续时间和高病毒载量的持续时间。研究将1505名受试者随机分为两组,分别皮下注射REGEN-COV 1200 mg或安慰剂,受试者的RT-qPCR检测与血清学检测均为阴性,且均预计与新冠感染者一起生活至少28天。研究结果显示,对于有症状的感染,REGEN-COV组感染率为1.5%(11/753),安慰剂组为7.8%(59/752),相对风险降低81.4%,优势比为0.17,P<0.001。对于所有有症状感染和无症状感染,REGEN-COV组感染率为4.8%(36/753),安慰剂组为14.2%(107/752),相对风险降低66.4%,优势比为0.31,P<0.001。图示有症状感染的发生率,可以看到REGEN-COV组(红色)明显低于安慰剂组(蓝色)在确诊有症状感染的患者中,REGEN-COV组症状缓解的平均时间1.2周,安慰剂组为3.2周。图示平均症状持续时间,可以看出REGEN-COV组(红色)明显低于安慰剂组(蓝色)在确诊有症状感染的患者中,REGEN-COV组高病毒载量的患者为1.6%(12/745),安慰剂组为11.3%(85/749),相对风险降低85.8%,优势比为0.13;P<0.001。高病毒载量的平均持续时间,REGEN-COV组为0.4周,安慰剂组为1.3周。图示高病毒载量的平均持续时间,可以看出REGEN-COV组(红色)明显低于安慰剂组(蓝色)总的来说,皮下注射REGEN-COV可以在一定程度上保护密切接触者不被感染,同时减少被感染者的症状持续时间和高病毒载量的持续时间。同时,该研究证明了皮下注射REGEN-COV是有效的,具有可接受的安全性,并且可以减少静脉输注所需的医疗资源消耗。需要强调的是,REGEN-COV这项紧急授权仅限于新冠病毒暴露后的预防,而不能用于非暴露预防。也就是说,在身边没有新冠感染者的情况下,还是要打疫苗。